
врач акушер-гинеколог высшей категории, специалист по репродуктологии, клинической гемостазиологии, интегративной и антивозрастной медицине.
Введение
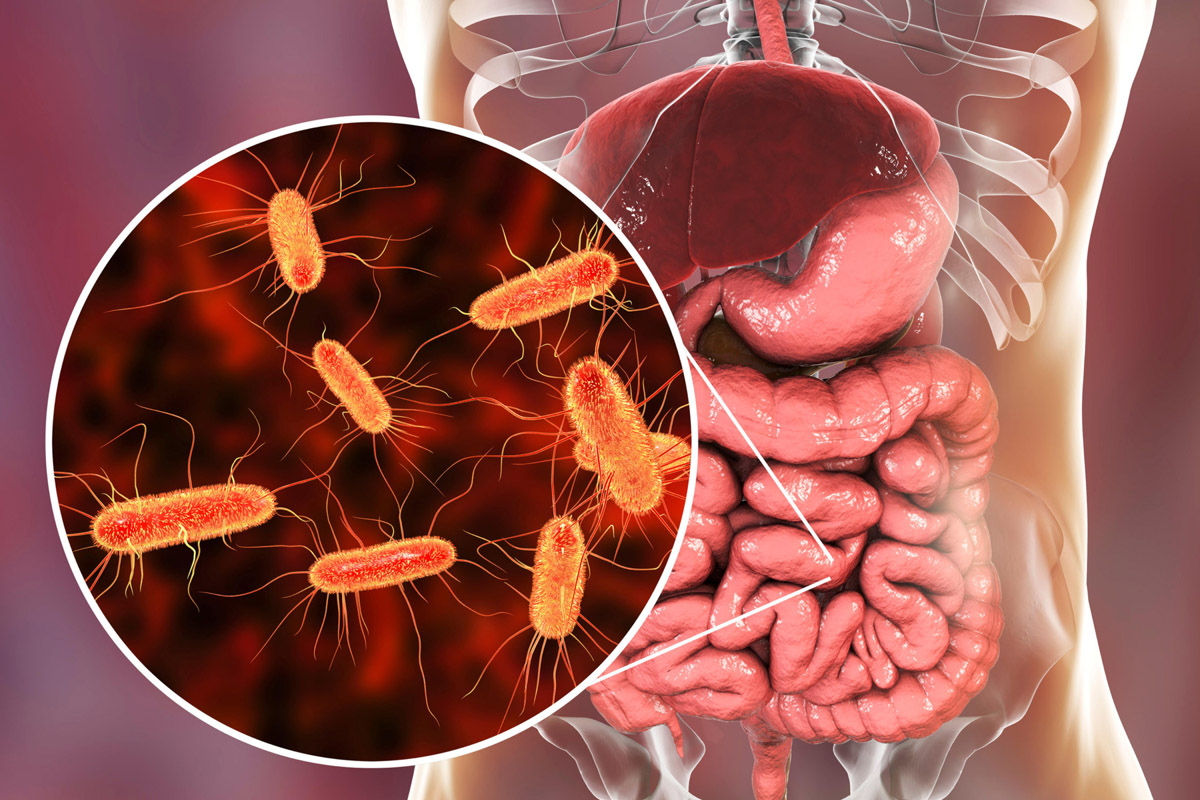
В классической клинической практике дисбактериоз часто рассматривается как локальная проблема ЖКТ, симптомокомплекс, ведущий к диспепсии или временному снижению иммунитета. Однако для специалиста антивозрастной медицины дисбиотические нарушения — это не фон, а один из центральных драйверов системного старения. Это отправная точка каскада патологических процессов: от хронического субклинического воспаления до ускоренной деградации кожи и когнитивных функций. Современные исследования, включая масштабные мета-анализы и работы в рамках проектов по изучению микробиома человека, убедительно доказывают: микробиота кишечника выступает в роли виртуального эндокринного органа, активного участника метаболизма и ключевого модулятора иммунитета.

ВЕБИНАР
Истощенный и депрессивный
человек
Определение дисбактериоза и его причины
В антивозрастном подходе мы уходим от упрощенного определения «дисбактериоз — это нарушение соотношения бактерий». Мы рассматриваем его как нарушение баланса в сложной экосистеме, ведущее к потере микробного разнообразия, сдвигу в соотношении фирмикутов и бактероидов, снижению численности симбионтов (таких как Faecalibacterium prausnitzii) и увеличению условно-патогенных штаммов. Это состояние эубиоза, при котором микробиом не может выполнять свои регуляторные функции.
Причины носят кумулятивный характер:
- Фармакологическая агрессия: Антибиотики — наиболее очевидный фактор, но не менее значимы длительный прием ИПП (ингибиторов протонной помпы), НПВП, оральных контрацептивов.
- «Западный» тип питания: Дефицит пищевых волокон — субстрата для ферментации — при избытке рафинированных углеводов, сахаров и насыщенных жиров.
- Хронический стресс: Кортизол напрямую влияет на проницаемость кишечного барьера и состав флоры.
- Экотоксины: Пестициды, тяжелые металлы, пищевые добавки (эмульгаторы) обладают доказанным микробиом-модулирующим действием, часто негативным.
- Возрастное истощение микробиоты (микробиотическое старение): Естественное снижение разнообразия и резистентности после 60-65 лет, которое можно и нужно замедлить.
Для anti-age врача выявление и нивелирование этих причин — первичная задача, предшествующая назначению любых добавок.
Значение микробиома для поддержания здоровья
Здоровый микробиом — это не пассивный «сожитель», а активный партнер в поддержании гомеостаза. Его ключевые функции, значимые для антивозрастной медицины:
- Метаболическая: Ферментация неперевариваемых волокон с производством короткоцепочечных жирных кислот (КЦЖК: ацетат, пропионат, бутират). Бутират — основной источник энергии для колоноцитов, ключевой эпигенетический регулятор (ингибитор гистондеацетилаз) и противовоспалительный агент.
- Защитная: Конкуренция с патогенами за ресурсы и рецепторы, поддержание целостности кишечного барьера.
- Иммуномодулирующая: Обучение и «настройка» врожденного и приобретенного иммунитета (до 70-80% иммунных клеток организма ассоциировано с кишечником).
- Синтетическая: Производство витаминов (К, В12, биотин, фолаты), нейротрансмиттеров (серотонин, ГАМК), конъюгация желчных кислот.
Потеря микробного разнообразия ведет к сбою во всех этих системах, что создает идеальную почву для ускоренного старения.

Как микробиота влияет на иммунную систему
Роль кишечных бактерий в защите организма
Слизистая оболочка кишечника — крупнейший иммунный орган человека. Комменсальные бактерии постоянно контактируют с иммунными клетками (дендритными клетками, макрофагами) через паттерн-распознающие рецепторы (TLR, NLR). Этот диалог поддерживает состояние контролируемой физиологической готовности — тренированный иммунитет. Симбионты стимулируют выработку IgA, регуляторных T-лимфоцитов (Treg), которые подавляют избыточные реакции. При дисбактериозе этот диалог искажается. Снижение численности продуцентов КЦЖК, особенно бутирата, ведет к ослаблению дифференцировки Treg-клеток. Напротив, условно-патогенная флора (например, некоторые штаммы E. coli, Bacteroides fragilis) может стимулировать провоспалительные Th1/Th17-пути. Первым клинически значимым следствием является не локальное воспаление в кишке, а системный «иммунный дисбаланс», проявляющийся в повышении уровня провоспалительных цитокинов в крови.
Хроническое воспаление и ускорение старения тканей
Этот системный цитокиновый подъем — основа феномена «инфламэйджинга» — хронического вялотекущего воспаления, признанного одной из главных причин старения. Провоспалительные маркеры (IL-6, IL-1β, TNF-α, CRP) напрямую воздействуют на все ткани:
- Активируют NF-kB-путь в клетках, что ведет к продукции еще большего количества медиаторов воспаления и подавлению аутофагии — процесса клеточного «очищения».
- Индуцируют клеточное старение (сенесценцию): Стареющие клетки перестают делиться, но остаются метаболически активными, секретируя провоспалительный SASP-фактор (феномен «зомби-клеток»), усугубляя порочный круг.
- Подавляют функцию стволовых клеток, снижая регенеративный потенциал тканей.
Таким образом, дисбактериоз, запуская иммунный дисбаланс, становится триггером инфламэйджинга — универсального механизма повреждения, лежащего в основе возраст-ассоциированных заболеваний: от атеросклероза и артрита до нейродегенерации.

Связь дисбактериоза и окислительного стресса
Нарушение метаболических процессов
Окислительный стресс — дисбаланс между производством реактивных форм кислорода (АФК) и возможностью антиоксидантной системы их нейтрализовать. Дисбиоз напрямую влияет на оба компонента. Во-первых, патогенные бактерии и их компоненты (например, липополисахариды, ЛПС) активируют в иммунных клетках NADPH-оксидазу, ведущий фермент для генерации АФК. Во-вторых, здоровый микробиом сам является источником эндогенных антиоксидантов (например, молочная кислота, бутират обладают антиоксидантными свойствами) и стимулятором синтеза глутатиона — главного клеточного антиоксиданта. При дисбактериозе эта функция угасает. Более того, нарушение ферментации и всасывания нутриентов ведет к дефициту витаминов-кофакторов антиоксидантных ферментов (цинк, селен, витамины С, Е).
Повреждение клеточных структур и ДНК
Избыток АФК, генерируемый на фоне дисбактериоза и сопутствующего воспаления, атакует все клеточные структуры:
- Перекисное окисление липидов мембран митохондрий и других органелл, что нарушает энергообразование и ведет к митохондриальной дисфункции — краеугольному камню старения.
- Окислительная модификация белков, включая коллаген и эластин, приводящая к потере их структурной целостности.
- Повреждение ДНК (разрывы цепей, окисление нуклеотидов). Накопление повреждений ДНК — прямой путь к геномной нестабильности, активации онкогенов и ускоренному клеточному старению.
Таким образом, дисбактериоз создает прооксидантную среду, которая ускоряет износ клеточного здоровья на фундаментальном уровне.

Влияние дисбактериоза на кожу и внешнее старение
Нарушение барьерной функции кожи
Системное воспаление и окислительный стресс, индуцированные дисбактериозом, нарушают дифференцировку кератиноцитов и синтез липидов рогового слоя. Это ослабляет эпидермальный барьер, увеличивает трансэпидермальную потерю влаги (ТЭПВ) и делает кожу более реактивной, чувствительной, склонной к розацеа и акне взрослых — состояниям, усугубляющим фотостарение.
Снижение синтеза коллагена и эластина
Провоспалительные цитокины (в частности, IL-1β, TNF-α) напрямую подавляют синтез коллагена I и III типа фибробластами и активируют матриксные металлопротеиназы (ММП), особенно MMP-1 (коллагеназу) и MMP-9 (желатиназу). Окислительный стресс также активирует ММП через фактор транскрипции AP-1. Результат — катаболизм коллагена и эластина начинает преобладать над анаболизмом задолго до естественного возрастного снижения.
Преждевременное образование морщин
Суммарный эффект — ускоренное разрушение внеклеточного матрикса, обезвоживание, потеря тонуса и упругости. Кожа стареет не по «генетическому плану», а под влиянием внутренней провоспалительной и прооксидантной среды, созданной в кишечнике. Это объясняет, почему даже при интенсивном внешнем антивозрастном уходе (сыворотки, пилинги) результат может быть нестойким без коррекции внутреннего статуса.

Коррекция микробиоты для замедления старения
Диетические подходы: пробиотики и пребиотики
Пребиотики — основа стратегии.
Это не синоним пищевых волокон, а их определенные типы, избирательно ферментируемые полезной флорой (инулин, фруктоолигосахариды (ФОС), галактоолигосахариды (ГОС), резистентный крахмал). Их источниками являются корень цикория, топинамбур, лук-порей, чеснок, зеленые бананы, охлажденный вареный картофель/рис. Задача — обеспечить субстрат для эндогенных симбионтов. Дозировка и постепенное введение критически важны для избежания вздутия.
Пробиотики — тактический инструмент.
Их выбор должен быть обоснованным. Штаммы Lactobacillus и Bifidobacterium эффективны для поддержки барьера и модуляции иммунитета. Однако в случаях тяжелого дисбиоза, после антибиотиков или при СИБР (избыточном бактериальном росте в тонкой кишке) их назначение требует осторожности. Новое поколение — пробиотики на основе Akkermansia muciniphila (укрепляет мукозальный слой) или Faecalibacterium prausnitzii (бутират-продуцент) — показывают огромный потенциал в исследованиях, но требуют дальнейшего изучения. Консенсус ESCOP (European Scientific Cooperative on Phytotherapy) и международные клинические рекомендации подчеркивают важность выбора штамма под конкретные задачи (например, Lactobacillus rhamnosus GG для барьера, Saccharomyces boulardii при антибиотико-ассоциированной диарее).
Постбиотики и метабиотики
Бутират в форме бутирата кальция/магния, другие КЦЖК — это перспективное направление прямой доставки полезных метаболитов, минуя необходимость в определенных бактериях.
Формирование режима питания и образа жизни
- Хроно-питание: Соблюдение 12-14-часового ночного «окна» без пищи (интервальное голодание в мягком режиме) дает микробиоте период покоя, способствует аутофагии и улучшает ее состав.
- Разнообразие растительной пищи: Цель — 30+ различных растительных продуктов в неделю (овощи, фрукты, зелень, орехи, семена, специи). Это главный фактор увеличения альфа-разнообразия микробиома.
- Управление стрессом: Техники медитации, адекватный сон — поскольку стрессовые гормоны напрямую изменяют состав флоры.
- Разумная физическая активность: Умеренные аэробные нагрузки увеличивают количество бутират-продуцентов, тогда как чрезмерные интенсивные нагрузки могут усилить проницаемость кишечника и воспаление.

Заключение
Дисбактериоз в антивозрастной медицине — это системный патологический процесс, ведущий драйвер инфламэйджинга и окислительного стресса. Влияние нарушенной микробиоты кишечника выходит далеко за пределы ЖКТ, затрагивая иммунитет, метаболизм, клеточное здоровье и внешний вид кожи.
Механизмы дисбактериоза включают ослабление кишечного барьера, повышение уровня ЛПС, хроническую активацию иммунитета, повреждение ДНК и подавление синтеза коллагена. Его коррекция должна быть комплексной: приоритет — пребиотики и персонализированное питание, затем — адресное применение пробиотиков и других метаболитов.
Значение профилактики нарушений микробиоты
Для врача, практикующего антивозрастную медицину, поддержание эубиоза — не разовая акция, а непрерывная стратегия продления здоровья. Профилактика дисбактериоза через образ жизни и питание — более эффективный инструмент, чем последующая коррекция. Интеграция анализа состава микробиоты (например, методом полногеномного секвенирования) в рутинный чек-ап пациента 35+ позволяет выявить нарушение баланса на доклинической стадии и предпринять превентивные меры. Это и есть суть предиктивной, превентивной и персонализированной медицины, которую продвигает наша школа, — действовать не на уровне симптома, а на уровне фундаментальных механизмов старения.
Список использованной литературы:
- Clemente, J. C., et al. (2012). The impact of the gut microbiota on human health: an integrative view. Cell.
- Integrative HMP (iHMP) Research Network Consortium. (2019). The Integrative Human Microbiome Project. Nature.
- Franceschi, C., et al. (2018). Inflammaging: a new immune–metabolic viewpoint for age-related diseases. Nature Reviews Endocrinology.
- Rinninella, E., et al. (2019). What is the Healthy Gut Microbiota Composition? A Changing Ecosystem across Age, Environment, Diet, and Diseases. Microorganisms.
- Salem, I., et al. (2018). The gut microbiome as a major regulator of the gut-skin axis. Frontiers in Microbiology.
- Сonsensus documents of the International Scientific Association for Probiotics and Prebiotics (ISAPP) on the definition and scope of prebiotics, probiotics, postbiotics etc.
- Zhang, P. (2022). Role of oxidative stress in the pathogenesis of aging and age-related diseases. Aging and Disease.
- Morais, L. H., et al. (2021). The gut microbiota–brain axis in behaviour and brain disorders. Nature Reviews Microbiology.
- ESCOP Monographs: The Scientific Foundation for Herbal Medicinal Products (sections on probiotics).
- Singh, V., et al. (2022). Dysregulated microbial fermentation of soluble fiber induces cholestatic liver cancer. Cell (как пример глубокого влияния ферментации на системное здоровье).
- Leulier, F., et al. (2017). Integrative Physiology: At the Crossroads of Nutrition, Microbiota, Animal Physiology, and Human Health. Cell Metabolism.
- Conz, A., et al. (2023). The role of butyrate in anti-inflammatory effects and aging prevention. Aging Clinical and Experimental Research.



